Ci occupiamo di diversi tipi di celle, batterie e soluzioni per sistemi di accumulo di energia,
Per richieste sui nostri prodotti, non esitate a contattarci e vi contatteremo entro 24 ore.

Ci occupiamo di diversi tipi di celle, batterie e soluzioni per sistemi di accumulo di energia,
Per richieste sui nostri prodotti, non esitate a contattarci e vi contatteremo entro 24 ore.
Se vi siete mai chiesti perché le batterie agli ioni di litio vengono utilizzate negli smartphone e nei veicoli elettrici, la risposta risiede nella loro incredibile densità energetica.
Immagina una batteria come un sistema con due serbatoi separati di "particelle di energia" (ioni di litio).Ricaricaspinge le particelle da un serbatoio all'altro, immagazzinando energia.Scaricareli lascia fluire nuovamente, rilasciando quell'energia per alimentare il tuo dispositivo.
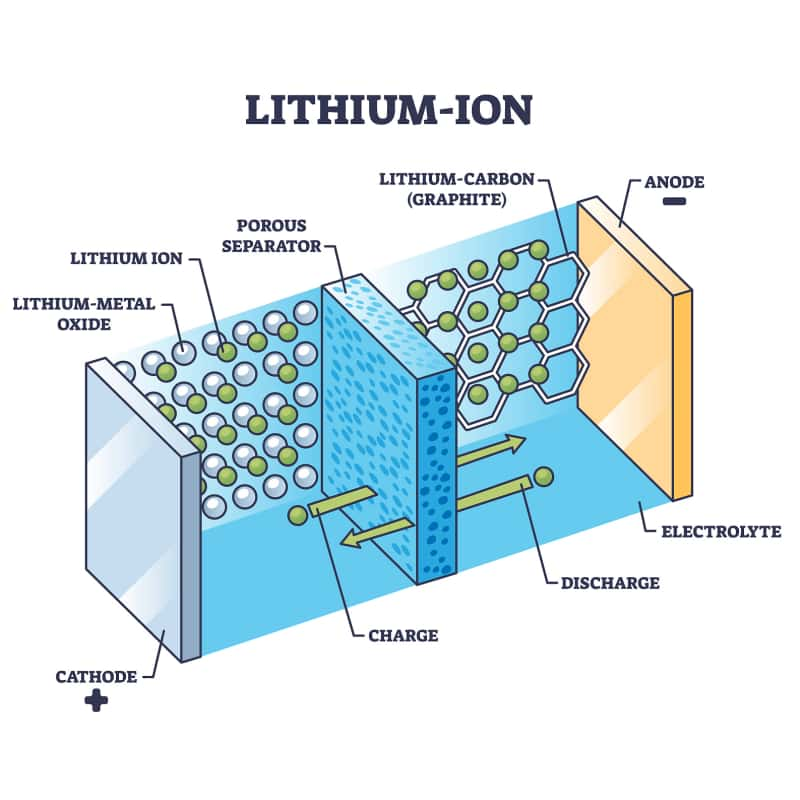
Anodo (elettrodo negativo):Di solito fatto digrafite(carbonio). Questo è il "serbatoio" in cui vengono immagazzinati gli ioni di litio quando la batteria è carica.
Catodo (elettrodo positivo):Realizzato in ossido metallico di litio (come l'ossido di litio-cobalto o il litio-ferro-fosfato). Questo è l'altro "serbatoio".
Qual è il ruolo dell'elettrolita in una batteria agli ioni di litio?:Un liquido o gel che si trova tra l'anodo e il catodo. Permetteioni di litioper attraversarlo, ma bloccaelettroni(questa è la chiave!).
Separatore:Una membrana porosa all'interno dell'elettrolita che impedisce all'anodo e al catodo di toccarsi (causando un cortocircuito).
Circuito esterno:Il filo o il percorso che collega l'anodo e il catodo all'esterno della batteria. È qui cheelettroniflusso per alimentare il tuo dispositivo.
Quando accendi il tuo dispositivo, chiudi il circuito e inizia spontaneamente una reazione chimica.
Viaggio degli ioni di litio:Ioni di litio immagazzinati nelanodo di grafitestaccarsi e nuotare attraverso ilelettrolitaalcatodo.
Gli elettroni prendono la strada panoramica:Per ogni ione che si muove, un elettrone viene rilasciato dall'anodo. L'elettrolita blocca gli elettroni, quindi sono costretti a prendere ilcircuito esterno(attraverso i componenti del telefono) per arrivare al catodo. Questo flusso di elettroniè elettricità, alimentando il tuo dispositivo.
Riunione:A livello del catodo, gli elettroni e gli ioni di litio si riuniscono e si incorporano nel materiale del catodo.
Riepilogo delle dimissioni:Anodo (grafite + litio)→Elettroni (dispositivo di potenza) + Li⁺ (attraverso l'elettrolita)→Catodo (Li si ricombina)
L'energia viene rilasciata.
Collegando il dispositivo si applica una forza elettrica esterna che spinge il sistema in retromarcia.
La potenza esterna spinge gli elettroni:Il caricabatterie forza il flusso di elettroniIndietrodal catodo all'anodo.
Ioni di litio Segui:In questo modo gli ioni di litio vengono estratti dal materiale del catodo, costringendoli a tornare indietro attraverso l'elettrolita fino all'anodo.
Magazzinaggio:Gli ioni si reinseriscono nella struttura di grafite dell'anodo, pronti per il successivo ciclo di scarica.
Riepilogo addebiti:Catodo (Li)→Li⁺ (forzata attraverso l'elettrolita dal caricabatterie)→Anodo (grafite + litio)
L'energia viene immagazzinata.
Immagina una ruota idraulica che aziona un mulino:
Lo Stato Caricato:Tutta l'acqua (ioni di litio) è nelsecchio superiore (anodo). Questo rappresenta l'energia immagazzinata.
Scaricamento:Si apre il cancello. L'acqua scorre giù dal secchio superiore, attraverso ilruota idraulica (il tuo dispositivo), nelsecchio inferiore (catodo)La ruota idraulica che gira funziona.
Ricarica:Si utilizza una pompa (il caricabatterie) per forzare l'acqua dal secchio inferiore a quello superiore, immagazzinando nuovamente energia.
Lasciate un messaggio
Scansione su Wechat :

Hi! Click one of our members below to chat on